Оглавление:
Влияние ионной силы раствора на растворимость
В присутствии посторонних ионов, создающих вокруг ионов осадка ионную атмосферу, но не вступающих с ними в химические реакции, 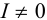 , и, согласно выражению (6.3), наблюдается увеличение растворимости осадка вследствие уменьшения знаменателя, называемое “солевым эффектом”. В этом случае, а также при достаточно большой концентрации собственных ионов, т. е. при высоком значении
, и, согласно выражению (6.3), наблюдается увеличение растворимости осадка вследствие уменьшения знаменателя, называемое “солевым эффектом”. В этом случае, а также при достаточно большой концентрации собственных ионов, т. е. при высоком значении 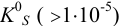 , учитывают ионную силу раствора и растворимость вычисляют по формуле (при
, учитывают ионную силу раствора и растворимость вычисляют по формуле (при 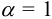 ):
):
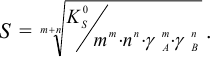
Пример 6.10.
Определить растворимость 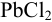 в воде.
в воде.
Решение:
Так как 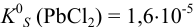 , что больше
, что больше 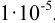 ,при расчете растворимости следует учесть влияние ионной силы раствора. Равновесие в системе выражается уравнением:
,при расчете растворимости следует учесть влияние ионной силы раствора. Равновесие в системе выражается уравнением:
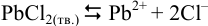
Из значения 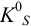 проведем оценку растворимости по формуле (6.4):
проведем оценку растворимости по формуле (6.4):
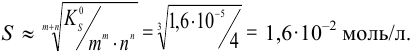
Ионную силу раствора вычисляем по формуле (2.1):
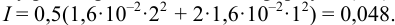
По табл. 1 приложения находим: 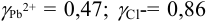 и рассчитываем растворимость хлорида свинца по формуле (6.8) с учетом ионной силы:
и рассчитываем растворимость хлорида свинца по формуле (6.8) с учетом ионной силы:
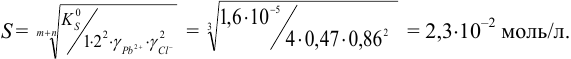
Проведенные вычисления свидетельствуют о возрастании растворимости вследствие влияния ионной силы.
Пример 6.11.
Сравните растворимость сульфата свинца в воде с растворимостью в 0,10 М растворе нитрата калия.
Решение:
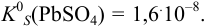 . Так как
. Так как 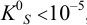 , при расчете ионной силы можно учесть только вклад сильного индифферентного электролита
, при расчете ионной силы можно учесть только вклад сильного индифферентного электролита 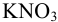 . Вычисляем ионную силу раствора:
. Вычисляем ионную силу раствора:
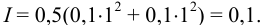
При этом 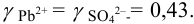 Рассчитаем растворимость хлорида свинца в водном растворе нитрата калия по формуле (6.8):
Рассчитаем растворимость хлорида свинца в водном растворе нитрата калия по формуле (6.8):
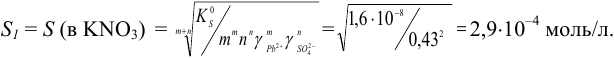
Растворимость 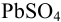 без учета ионной силы (в воде без
без учета ионной силы (в воде без 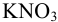 ):
):
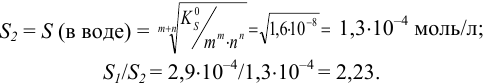
Вследствие «солевого эффекта» растворимость повышается в 2,23 раза.
Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Решение задач по аналитической химии
Возможны вам будут полезны эти страницы:

